当研究室で行っている研究のトピックを紹介しています。随時アップデートしていきたいと思います。
Nanopore sequencer and comprehensive diagnosis of infectious diseases
ナノポアシーケンサーと網羅的感染症診断
次世代シークエンサーの出現により、圧倒的に低コストで大量の塩基配列を解読することができる時代になり、あらゆる生命科学分野に革命をもたらしました。その中でも、特に我々が着目しているのがOxford Nanopore社から販売されているナノポアシーケンサーです。この手のひらサイズの小型シーケンサーはポータブルで、USBでノートパソコンに繋ぐことでシーケンスを行うことができます。我々は、この低コスト・ハイスループット・ポータブルなナノポアシーケンサーで、新しい感染症診断を行うことを目指しています。例えば患者さんや患畜の検体から病原体配列を濃縮し、網羅的に配列解読をすれば、病原体の感染状況について、今までより圧倒的に高い解像度で理解することができ、より最適な治療方針を決定することができるでしょう。これまでに分かっていなかった病原体が検出されることも期待されます。ナノポアシーケンサーは実験室や高価な機材がいらないため、どこでも(アフリカの僻地やジャングルでも!)簡単に遺伝子配列解読することができ、将来的に革新的な感染症診断ツールとなる可能性があると考えています。
当研究に関連した論文

Single cell level transcriptome analysis to understand heterogeneity in host - parasite interaction
単一感染細胞レベルでのトランスクリプトーム解析による宿主細胞と寄生虫の関係の多様性の理解
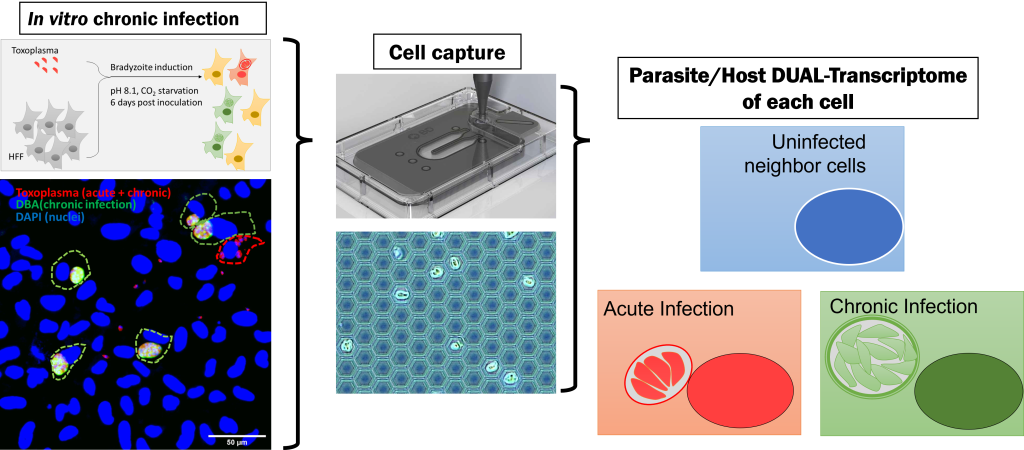
トキソプラズマ原虫は病態を引き起こす急性感染期と宿主間の移動や再活性化までの待機期間となりうる潜伏感染期を使い分けてヒトを含む哺乳類動物、鳥類に寄生する人獣共通感染症の病原体です。 地域により偏りはありますが、世界中でいまだにおよそ10%~30%程度の人口が感染しているとされています。特に免疫不全状態の患者(HIV陽性のAIDS発症患者)や妊娠中の感染による胎児への経胎盤感染から引き起こされる病態は時に致死的でありいまだに問題です。急性期において本原虫がどのように病態を引き起こすかについては研究が活発にされており、宿主の免疫系に働きかけ制御する原虫因子などの多くの病原関連因子が同定されています。 一方で潜伏感染状態のシストを含む食肉がヒトへの感染源となることからも潜伏感染期がどのように成立しているか知ることも本症の制御には必要です。トキソプラズマ原虫の潜伏感染は時に生涯にわたる感染といわれるほどの長期間にわたると報告されていますが、どのように原虫が宿主の免疫系の攻撃を逃れているのかは不明なところが多いです。 潜伏感染期の原虫と免疫系の応答を知るには、潜伏感染期において原虫が感染している宿主細胞の応答を見ることがはじめの一歩となります。 実際に原虫が感染している培養細胞のサンプルは潜伏感染期に至った原虫が感染している細胞、急性感染期の原虫を含む細胞、そして周囲の非感染状態の細胞などが混在する複雑系であり、「潜伏感染期の原虫による影響」を観察することは困難でした。 そこで私たちの研究室では、一つ一つの細胞を小さなくぼみ(nano-well)に振り分け、そのくぼみの中に入った細胞由来のRNAをくぼみに落としたビーズでトラップすることのできる系を利用して単一感染細胞レベルで宿主細胞のRNAと感染している病原体のRNAを同時に解析することを可能としました。 本解析により、急性感染期では宿主の細胞免疫応答が活性化していること、周囲の非感染細胞でも細胞免疫応答が活性化していること、しかしながら、潜伏感染期の虫体が存在する細胞では抑制されていることを明らかにすることができました。 潜伏感染期特有に抑制される免疫系シグナルは潜伏感染における宿主免疫系からの回避の一端を担うと考えており、その機序についてさらに解析を進めています。 トキソプラズマ原虫に限らず、寄生虫の感染は感染ステージをはじめ様々な場面で宿主細胞と関わり合いがあります、 単一感染細胞レベルでの解析を応用することで、それぞれの場面で寄生虫がどのように宿主細胞を利用しているのか、宿主細胞はどのように寄生虫の感染に対応しているのかを理解することにつながると期待しています。
On-site diagnostics for Neglected Tropical Diseases
顧みられない熱帯病に対するオンサイト遺伝子診断薬開発
アフリカトリパノソーマ症は野生動物や家畜から、ツェツェバエを介してヒトに感染する人獣共通感染症です。本症はサブサハラアフリカ地域における古くからの風土病で畜産業にも甚大な被害を与えていますが、アフリカにしか存在しない疾病のため診断薬や治療薬の開発が遅れ、いわゆる顧みられない熱帯病(Neglected Tropical Diseases: NTDs)の1つに挙げられています。トリパノソーマ症の診断は”顕微鏡観察”がスタンダードですが、顕微鏡観察だと原虫が少ない時に検出できないことや、そもそも熟練した技術者がいないと観察そのものが難しいといった課題がありました。遺伝子診断は高い感度で原虫を検出できますし、細かな種の鑑別も可能となります。そこで私たちの研究室では、60−65度程度で30分温めると原虫の遺伝子が増幅され、蛍光として観察できるLAMP診断系を開発しました。試薬は独自の方法で乾燥化しているため、電気やコールドチェーン(冷蔵・冷凍施設や輸送手段)がない場所でも使用可能で、簡便かつ高精度なアフリカトリパノソーマ症の現地での診断が可能となりました。当診断技術は種々の熱帯病診断に応用を進めています。